2013-10-22 | 编辑:文\先进制造部
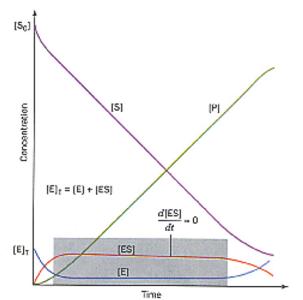
图1:反应过程中的拟稳态现象
生命系统中几乎所有的化学反应都有酶这种生物催化剂参与。对酶进行研究可以帮助人们更好的理解生命过程。酶动力学是研究酶催化反应速率的学科。它通过研究催化速率,以及催化速率在不同条件下的变化,来推断反应机制。早在1892年,Adrian Brown发现当蔗糖浓度高于酶浓度时,反应速率反倒与蔗糖浓度无关。在1902年,他提出这一现象可以由反应过程中形成了酶与底物的复合物来解释。在高底物浓度下,由于酶的供给相对较少,此时的酶都以复合物的形式存在。因此,进一步增加底物浓度并不能再增加复合物。而产物的生成速率与复合物的浓度有关,因而底物浓度的增加几乎不会影响反应物的生成速率。这一推断被认为是酶动力学的开端。
几乎同一时期,Victor Henri提出了两个单底物S单产物P反应机制模型。其中研究最广泛的一个,后来以Michaelis-Menten命名。Michaelis-Menten模型描述的是一个单底物单产物的酶催化过程。这一过程可以分解为两个基本反应,第一个简单反应是可逆过程,第二个简单反应是不可逆的。1925年,Briggs和Haldane提出了一个假设,拟稳态假设:在通常生理条件下,底物浓度远超过酶浓度时(S(0)>>E(0)),除反应起始阶段外,该阶段一般在E和S混和得几微秒之内,C保持近似常数,直至底物几乎耗尽。因而C合成的速率,在反应的大部分历程中必定与其消耗的速率相等,亦即C保持稳态,C可以当作常数来处理(图1)。
2008年,我们讨论了Michaelis-Menten模型中的拟稳态假设,证明了其正确性。论文发表在J. Phys. Chem. A 上。但是真实的生化过程是可逆的。研究不可逆模型是为了研究可逆模型。拟稳态假设在可逆模型中是否成立具有更重要的意义。上世纪三十年代以来,生物学家便认为拟稳态假设在可逆模型中是成立的,并一直使用至今。这一假设的基本重要性表现在它被写在各种生物化学和化学动力学教科书里。但是该假设一直没有得到严格的证明。本年度,我们证明了可逆模型中拟稳态假设仍是正确的。我们称其为可逆模型下的拟稳态定律。该文章被J. Math Chem 杂志接收,见:Bo Li, Banghe Li, Quasi-Steady-State Laws in reversible model of enzyme kinetics, Journal of Mathematical Chemistry, DOI 10.1007/s10910-013-0229-5.





